ENGINEERINGNET.BE - Bio-elektronische geneeskunde stimuleert elektrisch actief weefsel zoals zenuwen of spieren.
Meer bepaald het perifere zenuwstelsel (PZS) dat bestaat uit zenuwen die zich vertakken vanuit de hersenen en het ruggenmerg naar organen, ledematen en weefsels, is interessant voor bio-elektronische toepassingen, omdat het signalen van de hersenen naar de organen vervoert en vice versa. Door de cellen/zenuwen in het PZS elektrisch te stimuleren kan je zowel de hersenen als de organen bereiken.
Veelbelovende aanpak voor chronische aandoeningen
Ziektes in het PZS ontstaan als perifere zenuwen beschadigd zijn en daardoor de boodschappen tussen de hersenen en organen of weefsels niet correct kunnen doorgeven. Dat leidt tot problemen met spierbeweging, tast, temperatuur- en pijnervaring. Traditionele orale medicatie heeft vaak (neven)effecten over het hele lichaam en moet regelmatig aangepast worden om werkzaam te blijven.
Bovendien worden medicijnen vaak ontwikkeld voor een heel specifieke aandoening, terwijl PZS-ziekten een waaier van ziektebeelden omvatten. Bio-elektronische geneeskunde zou hier een mouw aan kunnen passen: doordat ze specifiek op de aangetaste zenuw werkt, blijven mogelijke bijwerkingen beperkt en lokaal. De therapie kan flexibel aangepast worden aan de noden van de patiënt. Het is een veelbelovende aanpak voor het behandelen van chronische aandoeningen zoals reumatoïde artritis, chronische pijn en epilepsie.
Technologische uitdagingen
Imec wendt zich tot nanotechnologie om de technologie achter de implantaten te verbeteren voor verschillende PZS-toepassingen, zodat ze kleiner en energiezuiniger worden. De imec wetenschappers werken aan steeds gedetailleerdere stimulatie, zoeken naar nieuwe materialen om de interne chip en elektronica van het implantaat te omhullen en zoeken naar een oplossing die signalen kan uitlezen en kan stimuleren wanneer nodig, op basis van geregistreerde signalen.
Specifiekere stimulatie
Een van de uitdagingen bij huidige PZS-technologie is de beperkte selectiviteit van de elektrische pulsen. Dit wordt belangrijker naarmate we meer complexe zenuwen willen stimuleren, zoals de nervus vagus. De nervus vagus is een zenuwbundel met een doorsnede van 4 mm. Ze bevat ook andere soorten vezels die zich vertakken en langs de zenuwen kronkelen. De juiste zenuw of vezel vinden is dus niet zo eenvoudig.
Daardoor kan stimulatie van nabijgelegen zenuwen onbedoelde lokale bijwerkingen teweegbrengen. Imec wetenschappers werken daarom aan een nieuwe techniek om de precisie van zenuwstimulatie te verbeteren gebaseerd op interferentiepatronen van elektrische velden met verschillende golflengtes. Dit zou niet alleen de therapie verbeteren, maar ook eventuele lokale neveneffecten drastisch kunnen verminderen.
Geavanceerde omhulsels voor implantaten
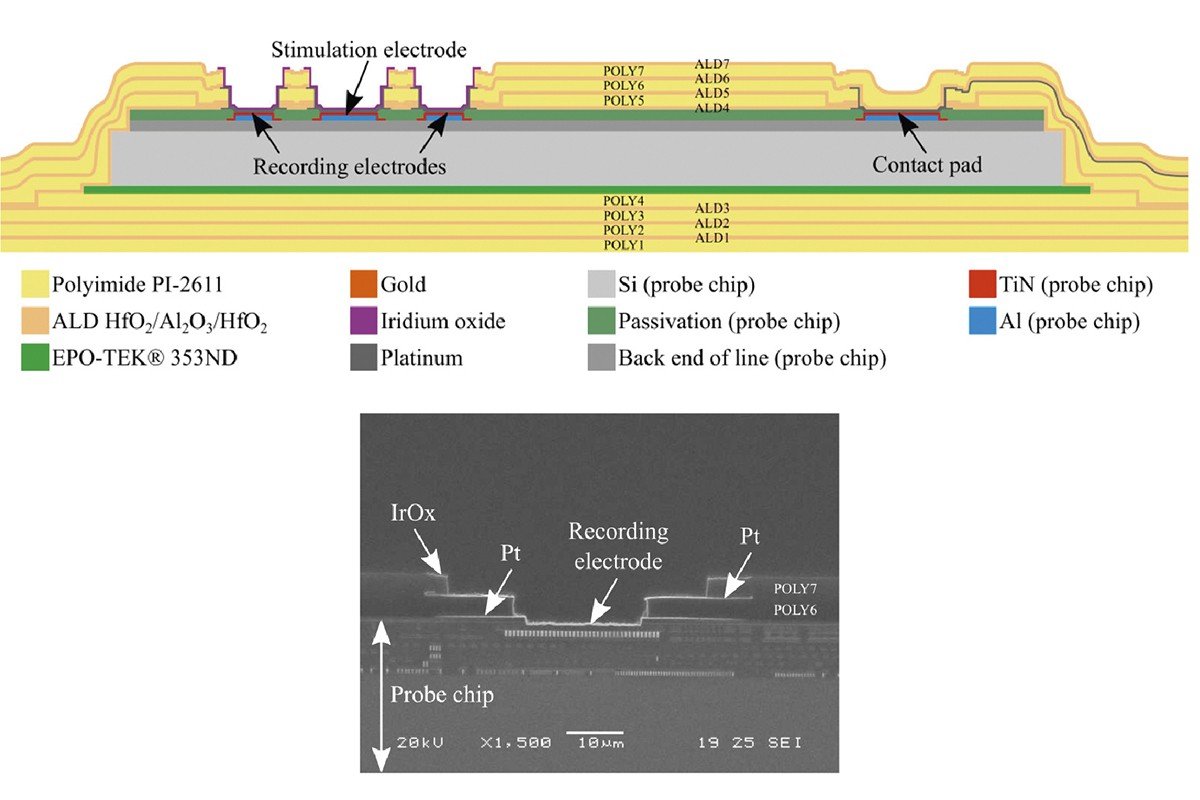
Een andere uitdaging is om een beschermende cocon te creëren voor het implantaat dat maandenlang, misschien zelfs jarenlang, in je lichaam zit. Traditioneel vertrouwen de meeste elektronische implantaten op robuuste omhulsels van rigide titanium. Maar titanium heeft beperkingen: het is rigide van structuur, en het is niet geschikt voor implantaten met micrometer afmetingen. CMST, een imec geassocieerd labo aan de Universiteit Gent, heeft een proces ontwikkeld om een PZS-implantaat te omhullen met behulp van dunne-film fabricagetechnieken.
Het resultaat is een zachte, flexibele verpakking die het kleinste implantaat kan afschermen, en tegelijkertijd een beter aanpassingsvermogen heeft aan het menselijke lichaam dan titanium. Voor het zachte omhulsel gebruikten de wetenschappers een unieke combinatie van polyimide, een polymeer dat al vaker voor dit doel gebruikt werd, en een combinatie van metaaloxiden aangebracht via atomaire laag depositie (ALD).
Zo wisselden ze 5.5 µm-dunne lagen polyimide af met ultradunne (10 - 20 nm) vochtafwerende coatings van metaaloxiden. Het resultaat is een opeenstapeling met het beste van beide werelden - de flexibiliteit van polyimide en de barrière-eigenschappen van ALD-lagen. Bovendien sluit elke stap van dit proces naadloos aan bij conventionele dunne-film fabricagetechnieken, waarmee de weg wordt geëffend voor grootschalige, kostenefficiënte productie.
Stimulatie op basis van uitgelezen informatie: een gesloten-lussysteem
Een van grootste uitdagingen voor toekomstige technologie is om de stimulatie aan te passen aan gemeten parameters, dus om een geslotenlus-systeem te creëren. Daardoor zou je bijvoorbeeld bij epilepsie alleen kunnen stimuleren als er een aanval gemeten wordt. Dat zou effectiever werken en onnodige stimulatie vermijden. In een nieuw project voor Horizon Europe, willen imec en de consortiumpartners, naar een implantaat dat signalen uitleest en op basis daarvan stimuleert.
Het implantaat zou in de stomp van een geamputeerde hand geplaatst worden en daar signalen in de armzenuwen uitlezen. Wanneer de patiënt denkt aan het bewegen van zijn hand, worden de uitgelezen signalen vertaald in beweging van de kunsthand. Feedback-informatie over bijvoorbeeld de positie, kracht, beweging van de kunsthand wordt vervolgens uitgelezen en als stimulatiepulsen doorgegeven aan de armzenuw. Zo ‘voelt’ de patiënt de beweging.
Een klein en energie-efficiënt implantaat
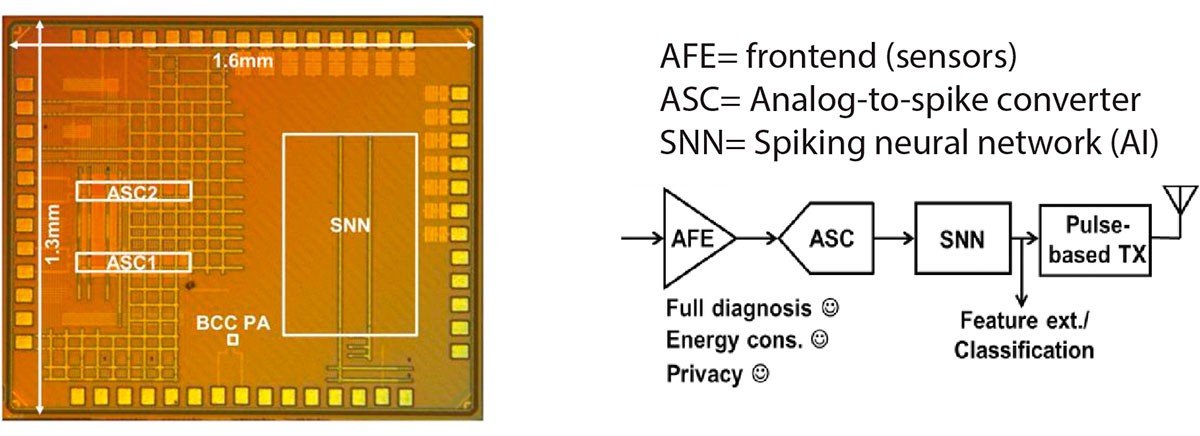
Om zulke gesloten-lussystemen te maken moeten nog enkele aspecten van de technologie geoptimaliseerd worden. Aangezien er vaak geen ruimte is voor een batterij moet het systeem zo weinig mogelijk energie verbruiken (veel minder dan 100 µW), om draadloze stroomvoorziening mogelijk te maken. Dat is niet eenvoudig voor systemen die verschillende functies combineren zoals signaalregistratie en stimulatie.
Een van de manieren om het energieverbruik te laten dalen is om alleen veranderingen te registreren in plaats van continue signaalregistratie. Een team in imec Nederland heeft dit idee onlangs vertaald naar een chip die alleen actief is wanneer een verandering in zenuwsignaal plaatsvindt.
Een blik op de toekomst
Door aan al deze uitdagingen te werken wil imec bijdragen aan de bioelektronische implantaattechnologie van de toekomst, die kleiner en energiezuiniger is, goed verdragen wordt door het lichaam, en heel precies kan stimuleren.
Dat opent nieuwe paden naar bijvoorbeeld nervus vagusstimulatie of gesloten-lusstimulatie, die op haar beurt andere toepassingen en verbeterde therapieën mogelijk maken. Zo kan uiteindelijk technologie voor het PZS een flexibele, efficiënte en op-maat-gemaakte therapie worden voor patiënten met PZS-aandoeningen.



